StressMarq Biosciences Inc.品牌商
10 年
手机商铺
- NaN
- 0
- 0
- 2
- 2
推荐产品
公司新闻/正文
Nature 子刊:发现帕金森潜在治疗新靶点,或有望完全治愈
743 人阅读发布时间:2024-05-22 09:34
帕金森病(PD)是一种神经退行性疾病,据统计目前已影响全世界超过 1,000 万人,而我国 65 岁以上人群 PD 患病率就达到 1.6%~1.7%。帕金森病患者经常出现运动迟缓和僵硬等运动症状,以及便秘和睡眠障碍等非运动症状。此外随着疾病严重程度增加,患者的握力也会逐渐下降。已经成为继肿瘤、心脑血管疾病之后威胁中老年人健康的第三大杀手。由于目前对疾病的病因和治疗方法尚未完全明确,经典的药物或手术治疗并不能从根本上阻止疾病进展,所以探索新的疾病机制和治疗靶点迫在眉睫[1]。
2024 年 4 月份,渥太华大学等研究机构合作在著名期刊 Cell Death & Diseae 发表创新成果 Genetic and pharmacological reduction of CDK14 mitigates synucleinopathy,首次发现细胞周期蛋白激酶 CDK14 能够减轻 α 突触核蛋白的病理聚集,可作为帕金森病的潜在治疗靶点,为理解帕金森病的发病机制和药物开发提供新的方向[2]。
疾病研究怎么做?课题思路解析
01 如何建立帕金森病小鼠行为模型?
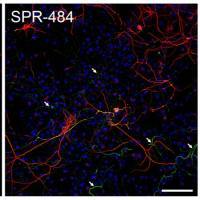
α 突触核蛋白是与帕金森病病理学相关的关键蛋白质。α 突触核蛋白高度磷酸化以及异常聚集形成的神经元内包涵体,也称路易体(LB),是疾病发生发展的罪魁祸首,导致神经毒性和神经退行性病变。在疾病研究中,注射 StressMarq 的小鼠源 Alpha 突触核蛋白前体原纤维(目录号 SPR-324 )或人源 Alpha 突触核蛋白前体原纤维(目录号 SPR-322),可导致小鼠大脑黑质中多巴胺能神经元的损失(这是帕金森病的决定性特点)并伴有轻度运动障碍,进而模拟 PD 患者的行为学特征。值得一提的是,给小鼠注射野生型 α 突触核蛋白原纤维,握力测试中前肢也会出现无力的症状。
02 鉴定疾病发生发展的潜在靶点
先前的研究使用混合 RNA 干扰(RNAi)筛选来研究果蝇中「可靶向的」α 突触核蛋白修饰因子,并将 CDK14 确定为一个潜在的驱动因子[3]。随后开展探究是否 CDK14 的遗传和药理学抑制可以减少小鼠和人类模型中的 α 突触核蛋白病理特征和帕金森病表型。
既往研究表明 CDK14 和 α 突触核蛋白基因(SNCA)在小鼠大脑中,特别是海马体和黑质(SN)中具有相似的基因表达模式。为了研究 CDK14 基因沉默在 α 突触核蛋白病中的作用,研究者给 CDK14 缺失的小鼠注射 StressMarq 的小鼠源 Alpha 突触核蛋白前体原纤维(目录号 SPR-324)或人源 Alpha 突触核蛋白前体原纤维(目录号 SPR-322)以建立帕金森病小鼠行为模型。研究发现 CDK14 基因沉默减轻了黑质中多巴胺能神经元的损失,并防止小鼠出现握力等行为缺陷。以此表明,CDK14 是帕金森病的潜在靶点。
03 CDK14 影响帕金森疾病进展的内在机制?
1. CDK14 基因沉默可减少磷酸化 α 突触核蛋白的病理聚集
研究表明磷酸化形式的 α 突触核蛋白(特别是 pS129)可促进 LB 形成。通过与健康人群比较,在帕金森病患者中发现这种病理标志物的水平明显升高。检测实验中所有鼠脑区域的 pS129 α 突触核蛋白阳性细胞,发现 CDK14 基因沉默减少了 pS129 α 突触核蛋白的病理聚集现象。此外,从携带帕金森病相关突变(A53T)的患者身上提取的多巴胺能神经元中,研究者也观察到了这种保护作用。
进一步对 α 突触核蛋白前体原纤维诱导的 PD 小鼠模型的大脑区域进行检测,惊奇地发现了相比于野生型小鼠,CDK14 基因沉默的小鼠中远离 α 突触核蛋白注射部位的区域,其 α 突触核蛋白病理聚集现象明显减弱,而注射端没有受到影响。这表明 CDK14 的缺失减少了 α 突触核蛋白的细胞间传播从而抑制病理性聚集扩散。
2. CDK14 药理学抑制可降低 α 突触核蛋白
最后,研究人员评估了 CDK14 的药理学抑制剂是否与 CDK14 基因消除具有相同的效果。研究人员采用了共价抑制剂(FMF-04-159-2)处理人类神经元,发现经 CDK14 抑制剂治疗的人类神经元其总 α 突触核蛋白水平呈剂量依赖性降低。对于体内实验,采用了过表达具有 PD 相关突变(A53T)的人 α 突触核蛋白的转基因小鼠模型。由于该模型只携带小鼠 SNCA 的部分等位基因,因此仅表达人类突变体 α-突触核蛋白,排除了所有其他 α-突触核蛋白的表达。结果显示 CDK14 抑制剂能够降低人类 α 突触核蛋白(突变的 A53T)蛋白水平,而不会给小鼠带来任何不良应激或疼痛。
04 广泛用于帕金森病小鼠模型研究的 StressMarq 相关产品
α 突触核蛋白基因(SNCA)的基因倍增和点突变(A53T)可导致 α 突触核蛋白过度表达和磷酸化,从而导致神经毒性。因此,降低 α 突触核蛋白的总水平和磷酸化是治疗帕金森病的一种有潜力的治疗策略。研究通过在小鼠模型中注射 StressMarq 的小鼠 Alpha 突触核蛋白前体原纤维(目录号 SPR-324)或人源 Alpha 突触核蛋白前体原纤维(目录号 SPR-322),重现帕金森病的病理和行为特征。利用细胞周期蛋白激酶 CDK14 基因沉默和药理学抑制的方法,证明抑制 CDK14 激酶具有神经保护作用并防止磷酸化 α 突触核蛋白病理性聚集,使帕金森病小鼠模型避免出现运动缺陷。总之,此研究表明抑制 CDK14 是治疗帕金森病的临床可行方案。
StressMarq 生产一系列用于神经退行性疾病研究的单体、寡聚和纤维状小鼠和人类 α 突触核蛋白结构。A53T 错义点突变(第 53 个氨基酸的丙氨酸被苏氨酸取代)与早发性帕金森病有关。StressMarq 的人源 A53T 突变阿尔法突触核蛋白前体原纤维(目录号 SPR-326)和单体(目录号 SPR-325)携带这种临床上重要的 A53T 突变。
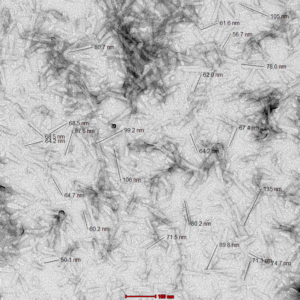
图 1. 小鼠重组前体原纤维(1 型)的 TEM(目录号 SPR-324)。
图片:100kx 放大倍数。
内容策划:邹礼平
内容审核:朱超敏
题图来源:图虫创意
文中图片来源:StressMarq
参考文献
[1] 黄镜璇,商慧芳. 帕金森病的病因和发病机制研究进展[J]. 中国实用内科杂志,2023,43(10):797-801,821.
[2] Genetic and pharmacological reduction of CDK14 mitigates synucleinopathy. Parmasad, L.A. et al. Cell Death & Disease. 2024.
[3] A druggable genome screen identifies modifiers of α-synuclein levels via a tiered cross-species validation approach. Rousseaux M.W.C., et al. J Neurosci. 2018.